Y creo que no exagero, porque compararlo con un mero bloque constructivo es quedarse corto. Muy corto. Las proteínas no sólo construyen todas las estructuras que nos componen, ni muchos menos. Participan en todos los procesos biológicos que podamos pensar, incluso en muchos que aún desconocemos. Es por eso que su conocimiento y entendimiento es tan importante hoy en día.
Por supuesto que tenemos proteínas obreras, como el colágeno de nuestros huesos y tendones, o la queratina que nos hace crecer el pelo y las uñas. Pero también las tenemos realizando otras funciones muy diversas e interesantes. Son capaces de regular nuestras funciones vitales (como la insulina con la glucosa), transportar sustancias que son vitales para nosotros (la hemoglobina no necesita de presentación) o defendernos de agentes externos (siendo los anticuerpos un buen ejemplo de ello). Pero de todas sus actividades, una que me parece fascinante es la actividad enzimática. Aquellas proteínas que desempeñan esta función, las enzimas, son capaces de reconocer moléculas ajenas a ellas, cómo si de una diminuta, precisa, específica y rapidísima máquina se tratase, y transformarlas en aquello que se necesita en cada momento. Un logro que estamos lejos de terminar de comprender y reproducir en el laboratorio para nuestro propio beneficio.
La historia de hoy va dedicada a ellas. En concreto, en esta entrada veremos un poco cómo los científicos de hoy, en un intento por comprender las habilidosas manos de la Madre Naturaleza, se las han ingeniado para estudiarlas de cerca. Se trata de la cristalización de proteínas. Veremos que ésto no es más que la formación de pequeños cristales formados, exclusivamente, por proteínas. Este año he tenido la experiencia, y el privilegio porqué no, de llevar a cabo este proceso. Veamos en qué consiste.
Primero, un poco de historia
Ya en la segunda mitad del siglo XIX, la cristalización de proteínas era un hecho. En aquel entonces permitía separarlas de una mezcla compleja o verificar si realmente se había purificado adecuadamente, además de ser una curiosidad científica más. De hecho, al principio la hemoglobina se cristalizaba por el mero hecho de poder hacerlo, sin mayor interés. Pero enseguida los científicos descubrieron que una buena cristalización permitía una cierta caracterización de las moléculas, ya que algunas presentaban patrones muy particulares. En las décadas de 1900 a 1940, con la importancia creciente de las nuevas enzimas descubiertas, la cristalización se convirtió en una herramienta muy útil. Por aquel entonces apareció la técnica más importante y que, hasta día de hoy, permite conocer los datos estructurales de una enorme cantidad de moléculas: la cristalografía de Rayos X. Como su propio nombre indica, utiliza radiaciones de elevada energía que, al difractarse a través de la red de un cristal, permite determinar las posiciones puntuales de los átomos que lo constituyen. El problema de esta técnica se encuentra precisamente ahí. La fabricación de cristales perfectos, los llamados monocristales, es una empresa harto difícil. En este sentido, debemos imaginarnos a nuestras enzimas como a pequeños prismas, del tamaño de unas pocas micras, que producen patrones de difracción característicos debido a su estructura sólida. Era obvio que se necesitaba un elevado conocimiento de cristalización para conseguir los ansiados monocristales y, de esta forma, estar un paso más cerca de ver de cerca a las proteínas. Pero no olvidemos que las proteínas son macromoléculas compuestas por miles y miles de átomos, con lo que encajarlos todos no es una tarea nada trivial, aún teniendo los datos del difractograma de Rayos X.
Este descubrimiento fue un logro sorprendente. Pero el gran cambio en la cristalización de proteínas se produjo en la década de 1980. Fue entonces cuando se pudo producir proteínas "a gran escala" gracias al desarrollo del ADN recombinante, lo cual era una fuente mucho más abundante para proteínas con las que, de otra forma, era prácticamente imposible trabajar. Un mayor número de proteínas accesibles significó a su vez un enorme desarrollo de la cristalografía de Rayos X y, por supuesto, de las técnicas de cristalización.

Así estamos a día de hoy. Hemos descubierto el genoma humano. Conocemos el funcionamiento de virus, desarrollamos medicinas, antibióticos. Hemos ido a la Luna, y hemos vuelto. Navegamos por la sociedad de la información como quién cruza la calle. Somos capaces de enviar sondas más allá de nuestro sistema solar para ver lo más lejano. Y, sin embargo, el mejor método para estudiar a nivel estructural las proteínas, unos entes diminutos, sigue siendo una técnica que ya se descubrió hace unos 80 años. Pero vamos a meternos un poco en faena. ¿Cómo hacen verdaderamente los cientificos para convertir un espaguetti molecular en una gema tan preciada?
Algunas recetas
La cristalización de proteínas se asemeja enormemente a esa típica receta de cocina que sólo acabas perfeccionando cuando la llevas practicando mucho tiempo. No sólo por su carácter protocolario. Hoy en día, la mayor parte de las cristalizaciones se realizan mediante la intuición, necesitan de paciencia y perseverancia. Y es que, en pleno siglo XXI, no acabamos de entender muy bien cuáles son los procesos fisico-químicos que favorecen la cristalización de las proteínas de una forma determinada. Como antes os comentaba, este tipo de macromoléculas cuentan con miles de átomos, con cientos de enlaces y miles de grados de libertad. Vamos, demasiada información para nuestros "bodies".
¿Dónde nos deja esto? Bueno, por suerte nuestra generación cuenta con un buen respaldo científico. La enorme cantidad de pruebas de ensayo-error nos han dado algunas ideas de cómo pueden funcionar los mecanismos de cristalización, y así se actúa en consecuencia. De todas formas, sacar conclusiones de los resultados obtenidos es otro cantar.
Aún así, contamos con técnicas de cristalización, bien creando una supersaturación de la disolución, bien disminuyendo la solubidad de la proteína. En general, todas se basan en alcanzar de una forma u otra un grado de supersaturación de la disolución de proteína, de forma que se formen unos pocos núcleos a partir de los cuales crecerán los cristales. Algunas tienen nombres tan extraños como los siguientes:
- Alteración de la constante dieléctrica del medio.
- Adición de un polímero que produzca exclusión volumétrica.
- Eliminación directa del agente disolvente.
- Evaporación.
- Microdiálisis.
- Equilibrio de vapor en gota colgante.
- Extracción secuencial.
- Cristalización inducida por cambios de pH o temperatura.
Con las manos en la masa
Vaya nombres, ¿eh?. Todo un galimatías, lo reconozco. Pero hay uno de todos ellos que, pese a tener un nombre un tanto ridículo, es realmente sencillo de entender. Precisamente fue el que realizamos en el laboratorio. Se trata del método de equilibrio de vapor en gota colgante. Vamos a ver de qué se trata.
Para ello, os propongo un ejercicio mental de abstracción. Suponeros que tenéis un recipiente con agua destilada y otro con agua salada. En vuestra inabarcable imaginación, suponed que cogéis de vuestro laboratorio imaginario un pequeño círculo de vidrio, parecido a una moneda. ¿Lo tenéis? Bien. Ahora colocad sobre él una gota del recipiente de agua destilada. Os recomiendo que utilicéis un gotero o pipeta, pero seguro que vuestra imaginación os da otras ideas.
Con mucho cuidado, dadle la vuelta a vuestro pequeño círculo de vidrio, de manera que la gota quede suspendida boca abajo. Rápidamente, y antes de que se caiga, debéis colocar dicha plaquita boca abajo sobre un recipiente lleno del agua salada que teníais. Si habéis seguido los pasos, debéis tener en vuestro laboratorio imaginario algo como ésto:
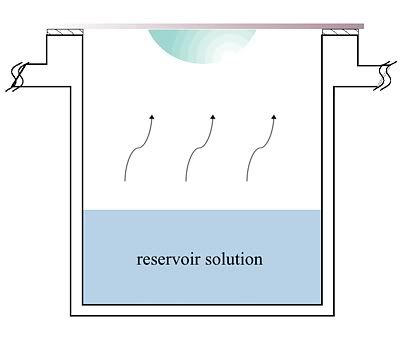
Ahora empieza la magia de la química y la física. Si recordáis, el agua destilada se encuentra en la gota, mientras que en el fondo del reservorio hay una "disolución" de agua salada. Existe, por tanto, una diferencia de concentración de sales entre ambos disolventes. Pues bien, esta diferencia de concentración crea el llamado potencial químico, que en definitiva provoca la migración de las sales desde la disolución más concentrada a la más diluida. La tendencia general es que ambas disoluciones tengan al final la misma concentración, hasta que el potencial químico de ambas disoluciones se iguale. Esto ocurre gracias al equilibrio de vapor, exactamente igual que ocurre cuando el salitre se acumula en las zonas costeras.
En esto consiste la técnica del equilibrio de vapor en gota colgante. Sólo debéis cambiar el agua destilada por la disolución de proteína que queráis cristalizar, y la de agua salada por una disolución con una cierta cantidad de agente precipitante. Dicho agente migrará hacia la gota, donde hará cristalizar de manera lenta y controlada los cristales de proteína. En nuestro caso, el tiempo que empleamos varió entre los 2 días y la semana para que se formaran una buena cantidad de cristales, y de tamaño "considerable".
Sencillo, ¿no?
El postre
Lo importante en la cristalización de proteínas no es el número, sino la calidad del producto. Recordemos que nuestro objetivo es realizar un estudio de difracción de Rayos X, el cual requiere de unas condiciones óptimas. Así, cuanto más grandes y perfectos sean los cristales, tanto de mayor calidad serán nuestros resultados. Por eso se hacen ensayos con diferentes agentes precipitantes hasta conseguir las mejores condiciones de precipitación, donde los cristales sean de gran tamaño y fáciles de aislar.
Con el permiso de mis compañeros de laboratorio, a los que agradezco enormemente este material, os voy a enseñar las fotografía de los cristales que obtuvimos este año en el laboratorio de prácticas. Se trata de una enzima llamada lisozima, presente en la clara del huevo.
El resultado no es muy profesional, pero muy vistoso. Los diferentes colores se deben a los filtros del propio microscopio, que permiten distinguir las caras de los prismas. Enhorabuena a todos mis compañeros, por vuestra habilidad como joyeros microscópicos.
Referencias: McPherson, Alexander. Introduction to protein crystallization. Methods 34 (2004) 254-265.